Les patients attendent d’un antalgique aigu qu’il soulage leur douleur rapidement et efficacement. Deux méthodes principales permettent d’y parvenir et de continuer à améliorer les antalgiques contenant de l’ibuprofène, un principe actif éprouvé : l’associer à d’autres substances, telles que la caféine qui est un co-antalgique, ou formuler l’ibuprofène sous forme de sel de lysine pour accélérer son absorption dans la circulation sanguine (et ainsi soulager la douleur plus rapidement).
 France
FrancePropriétés pharmacocinétiques de l'ibuprofène : comparaison entre l'association à dose fixe d'ibuprofène plus caféine, le lysinate d'ibuprofène et l'acide d'ibuprofène
Résultats de deux études à dose unique (monocentriques, randomisées, croisées, en ouvert)
L’efficacité plus importante de l’ibuprofène (400 mg) plus caféine (100 mg) par rapport à l’ibuprofène (400 mg) seul a été clairement établie [1]. Deux études cliniques ont également porté sur les propriétés pharmacocinétiques de l’ibuprofène dans l’association et celles du lysinate d’ibuprofène, tous deux administrés à jeun (>10 h de jeûne) et suite à l’ingestion d’un petit-déjeuner standard [2].
Méthodologie
Deux études cliniques, portant chacune sur 36 sujets, ont été menées. Dans la première étude (NCT01879371), les propriétés pharmacocinétiques de l’ibuprofène utilisé en association à dose fixe avec de la caféine ont été comparées à celles de l’ibuprofène (sous forme d’acide ou de lysinate) contenu dans deux préparations de comparaison. Les préparations de l’étude ont été prises après >10 heures de jeûne, période au cours de laquelle les patients ont seulement été autorisés à boire de l’eau.
Dans la seconde étude (NCT02629354), les propriétés pharmacocinétiques de l’ibuprofène utilisé en association à dose fixe ont été comparées à celles de l’ibuprofène (sous forme de lysinate) suite à l’ingestion d’un petit-déjeuner standard.
Ces études à dose unique étaient monocentriques, randomisées, croisées et en ouvert. Les paramètres clés mesurés étaient les pics de concentration plasmatique (Cmax), le temps nécessaire pour les atteindre (Tmax) et l’exposition totale (AUC0-t). Ces paramètres ont également été mesurés pour la caféine. Les méthodes analytiques et statistiques correspondaient aux standards habituels [2].
Résultats
La prise à jeun a démontré les résultats attendus : l’ibuprofène sous forme de lysinate a été absorbé plus rapidement que l’acide d’ibuprofène (en association à dose fixe ou contenu dans la préparation à base d’ibuprofène seulement). Malgré une exposition comparable, les pics de concentration plasmatique étaient supérieurs (voir tableau).
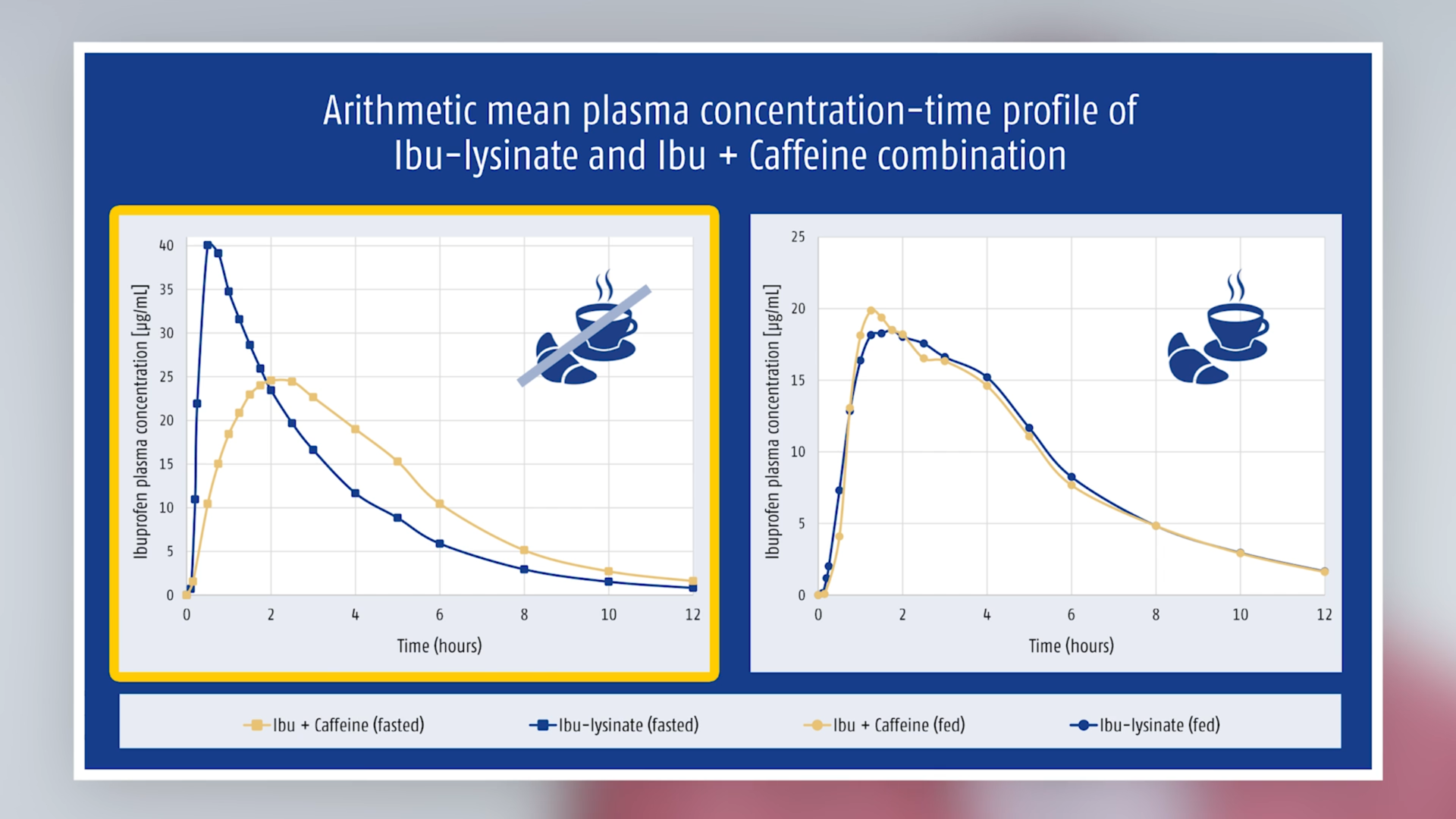
Il en va autrement après avoir pris un petit-déjeuner standard, c’est-à-dire lorsque l’estomac n’est pas à jeun : dans ces conditions, les concentrations plasmatiques de l’ibuprofène utilisé en association étaient supérieures à celles du lysinate d’ibuprofène et le temps nécessaire pour atteindre les pics de concentration plasmatique était plus court (voir tableau et illustration 1). La différence entre les états à jeun/non à jeun était également significativement moindre qu’avec le lysinate d’ibuprofène (illustration 2).
Ill. 1 Moyennes arithmétiques de l’évolution des concentrations plasmatiques en fonction du temps de l’ibuprofène et de la caféine en association à dose fixe.
Ill. 2 Moyennes arithmétiques de l’évolution des concentration plasmatiques en fonction du temps de l’ibuprofène (sous forme de lysinate).
Discussion et conclusions
Selon la définition de l’Agence européenne des médicaments, le terme « à jeun » signifie que la personne participant à une étude n’ingère rien pendant au moins 8 heures avant et 4 heures après la prise du produit de l’étude, boit seulement de l’eau plate et n’est pas autorisée à boire quoi que ce soit une heure avant et une heure après la prise. Les produits de l’étude doivent être pris avec exactement 150 ml d’eau [3]. Bien qu’elles soient très éloignées de la réalité, ces conditions standardisées permettent de comparer des études distinctes assez efficacement.
Les antalgiques sont rarement pris dans des conditions répondant aux exigences standard de la définition de « à jeun » donnée par les autorités de santé. Pour les respecter, une personne devrait prendre un antalgique avant le petit-déjeuner (et uniquement si le dîner n’avait pas été pris trop tard !) et devrait également sauter le petit-déjeuner lui-même. Ce sont les seules conditions dans lesquelles il est prouvé que l’ibuprofène sous forme de lysinate est absorbé plus rapidement (et que les pics de concentration plasmatique sont plus hauts) que l’acide d’ibuprofène. Des données plus anciennes ont montré qu’après un petit-déjeuner standard, le lysinate d’ibuprofène et l’acide d’ibuprofène ont des propriétés pharmacocinétiques comparables et donc, que le lysinate d’ibuprofène ne présente aucun avantage [4]. Une publication plus récente montre que l’ibuprofène en association avec de la caféine est absorbé plus rapidement par un estomac qui n’est pas à jeun et atteint des pics de concentration plasmatique plus élevés que le lysinate d’ibuprofène [2].
Références bibliographiques
- Weiser et al. Efficacy and safety of a fixed-dose combination of ibuprofen and caffeine in the management of moderate to severe dental pain after third molar extraction. Eur J Pain. 2018;22(1):28–38. doi: 10.1002/ejp.1068.
- Weiser et al. Pharmacokinetic Properties of Ibuprofen (IBU) From the Fixed-Dose Combination IBU/Caffeine (400/100 mg; FDC) in Comparison With 400 mg IBU as Acid or Lysinate Under Fasted and Fed Conditions-Data From 2 Single-Center, Single-Dose, Randomized Crossover Studies in Healthy Volunteers. Clin Pharmacol Drug Dev. 2019;8(6):742–753. doi: 10.1002/cpdd.672.
- EMA GUIDELINE ON THE INVESTIGATION OF BIOEQUIVALENCE, 2010 https://www.ema.europa.eu/en/documents/scientific-guideline/guideline-investigation-bioequivalence-rev1_en.pdf (accessed 05.12.2019)
- Klüglich et al. Ibuprofen extrudate, a novel, rapidly dissolving ibuprofen formulation: relative bioavailability compared to ibuprofen lysinate and regular ibuprofen, and food effect on all formulations. J Clin Pharmacol. 2015;45(9):1055–61.
Conflit d’intérêts : T. Weiser est employé chez Sanofi.
Divulgations: Publication financée par Sanofi Aventis Deutschland GmbH.